脂質ナノ粒子製造デバイス iLiNP
脂質溶液と薬剤溶液から脂質ナノ粒子 (リポソーム・ミセル) 製剤を連続的に製造するための、独自理論に基づき設計したマイクロ流路を持つデバイスです (国際特許出願番号PCT/JP2018/015550 出願人:北海道大学。ライラックファーマ株式会社は北海道大学より該当特許の独占使用許諾を得ています。)

リポソーム・ミセル ~魔法の超微小シャボン玉~
脂質と呼ばれる生体分子は水に溶けやすい頭部と溶けにくい尾部を持った構造をしており、一部の脂質は水の中で自己集合し膜を形成することが知られています。この膜が曲面を描いて球状になったものが、リポソームやミセルと呼ばれるものです。
シャボン玉の成分である界面活性剤も、実は脂質の仲間で、シャボン玉も界面活性剤の膜でできています。つまり、リポソームやミセルはシャボン玉の一種と言ってもよいわけですが、大きく違う点が2つあります。
1つ目は、球の中身が、シャボン玉では空気ですが、リポソームやミセルでは水などの液体が中に詰まっています。ということは、リポソームやミセルの中には、水などには溶けるけど膜は通らないものを封入することができます。
2つ目は、そのサイズで、リポソームやミセルはシャボン玉の1/10,000,000(1千万分の1)くらいの大きさ、具体的には10~200nm(ナノメートル:1ナノメートルは10億分の1メートル)しかありません。従って、リポソームやミセルの形は、目では見えません。電子顕微鏡などの特殊な装置が必要です。また、これほど小さいことから、人の体の隅々にまで入って行くことができます。
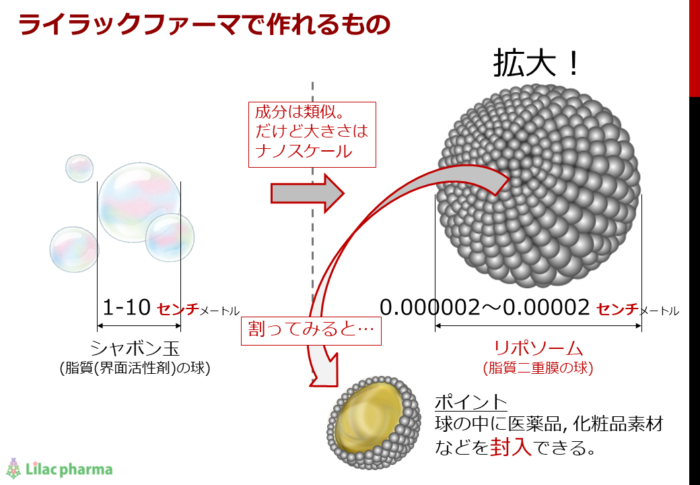
このリポソームやミセルの中に化粧品素材や医薬品を封入することで、内封物の患部への集積、効果の持続、副作用の低減等の効果が生じることが知られています。
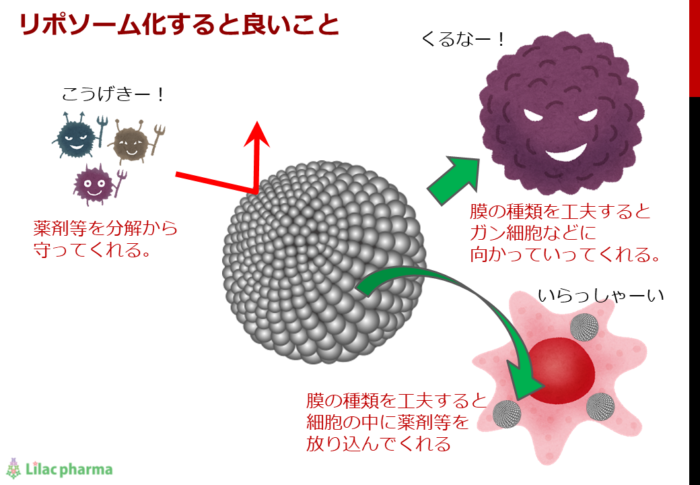
リポソーム・ミセルは粒径によってその能力が変わる
リポソームはその粒径が小さくなるほど、皮膚内部への浸透性が高まることが知られています。(DD. Verma et al., Int. J. Pharm., 258, 141-151 (2003))
他の例では、リポソームの平均粒径を100nm未満にすると、眼の強膜と呼ばれる外膜部分をリポソームが透過しやすくなることが知られています。(Joseph RR et.al. Nanomedicine (Lond.) (2017) 12(6), 683-702 :論文では豚の強膜を使用。)
また、脂質と似た分子構造を持つ人工ポリマーで作製したミセルは、その平均粒径が30nm以下になると組織内に染み渡り膵臓がんに届きやすくなることが知られています。(H. Cabral et al., Nat. Nanotechnol., 6, 815-823 (2011):論文では実験動物としてマウスを使用)
一方で、肝臓組織に対しては粒径が30nm近くになると粒径約70nmのものと比べて逆に広がりにくくなることが知られています(Y. Sato et al., J. Controlled Release, 229, 48-57 (2016))
これらの例のように、リポソームやミセルはその粒径によって浸透具合等を変えることができます。言い換えれば、粒径を精密にコントロールすることによって、その効果を最大にすることができます。
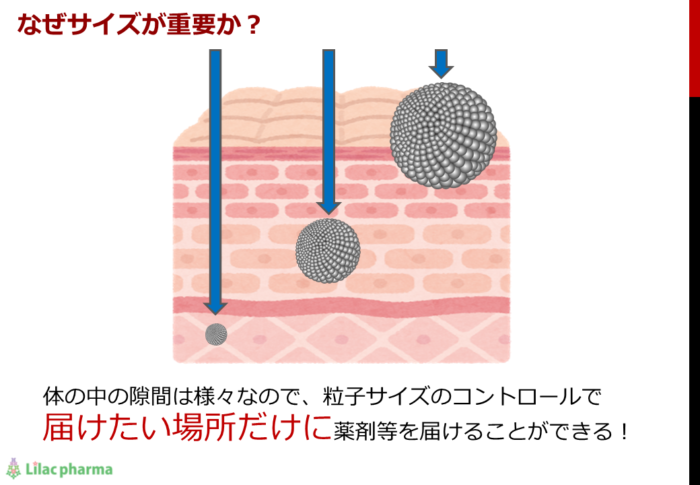
意外に難しい粒径制御
リポソームやミセルについては、いろいろな製造方法が知られていますが、工業的な大量生産に適するのはバッチ法と呼ばれているものです。おおよそのプロセスは次の通りです。最初に大小さまざまなリポソームを作ってから所定の大きさに揃えていく方法です。
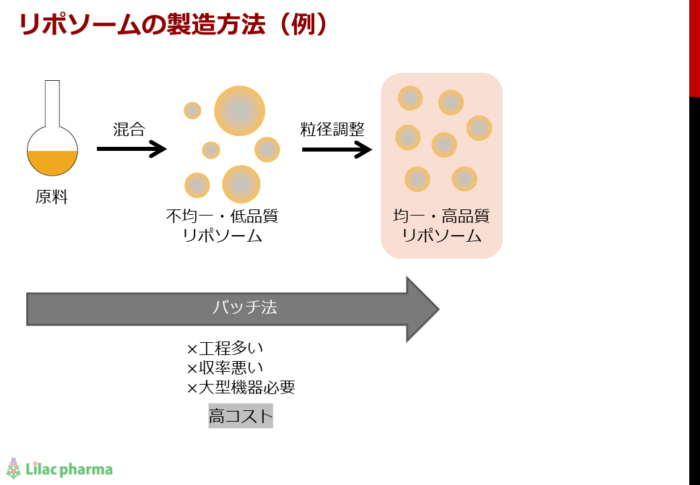
この方法では、最初のステップで大小さまざまな(通常は目標よりも大きな)リポソームが作られるため、その後に粒径調整を行う必要があります。
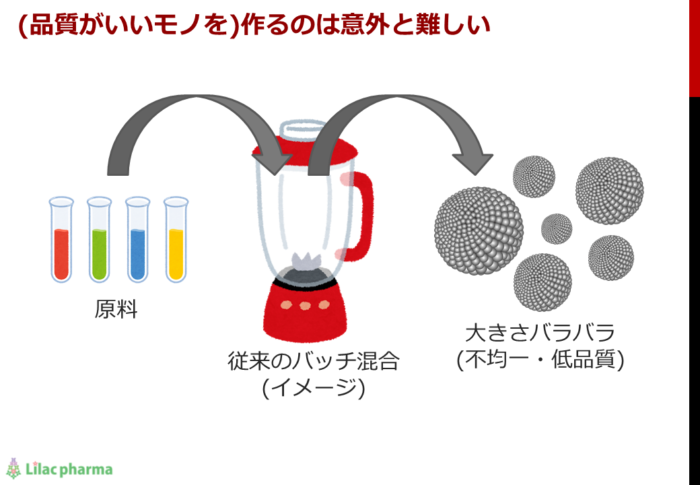
また再現性良く目標の粒径に合わせることも苦手で、安定した品質のリポソームを大量に作るには高度な技術が必要となります。
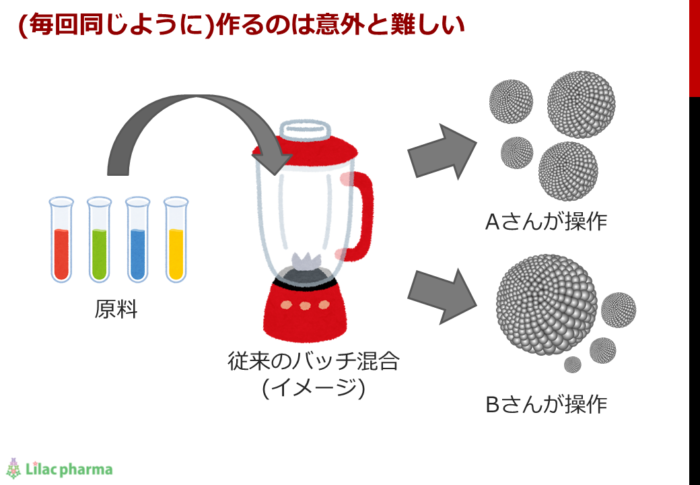
粒径コントロールを得意とする独自のマイクロ流路デバイス iLiNP
弊社でリポソーム・ミセルの製造に使用しているマイクロ流路デバイスiLiNPは、従来のバッチ法と異なり、原料から直接、目標の粒径のリポソーム・ミセルを製造するデバイスです。
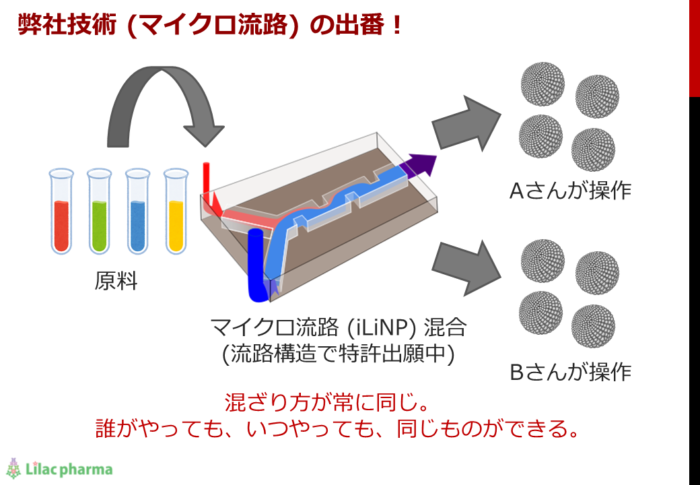
iLiNPではマイクロ流路と呼ばれる幅が数十~数百μm(マイクロメートル)の溝に原料を流し込み、ミリ秒単位の極めて早い時間で原料を混合(脂質溶液を希釈)しています。バッチ法での混合と比べて、リポソームやミセルの粒径がそれぞれバラバラに大きくなる時間的余裕が無いため、iLiNPから出てくるリポソームやミセルは最初から粒径が小さいリポソームになります。また細い流路内で均一に混合希釈するため、粒径の分布が狭い、高品質なリポソーム・ミセルが得られます。
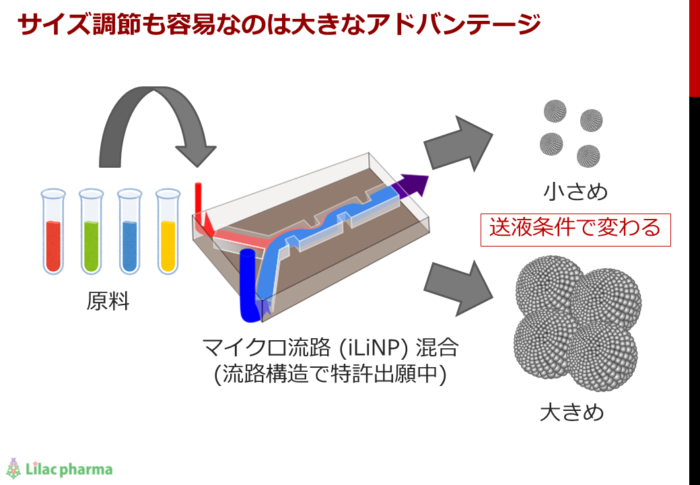
そして、iLiNPの最大の特徴は、流量(流速)を変えることでリポソームやミセルの粒径を自由にコントロールできるところです。原料を早く流せば小さい粒子が、遅く流せば大きい粒子が作られます。
既存のバッチ法では、これほどまで精密な粒径のコントロールは難しく、同分野の研究者にも認められている(アメリカ化学会の雑誌に論文受理・掲載されている)とてもユニークな特徴です。
iLiNPと従来法(バッチ法)の比較は次の通りとなり、iLiNPが多くの点で優位性を持つことがわかります。
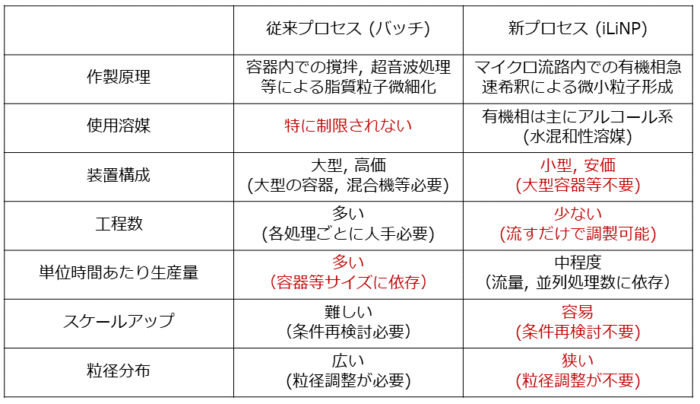
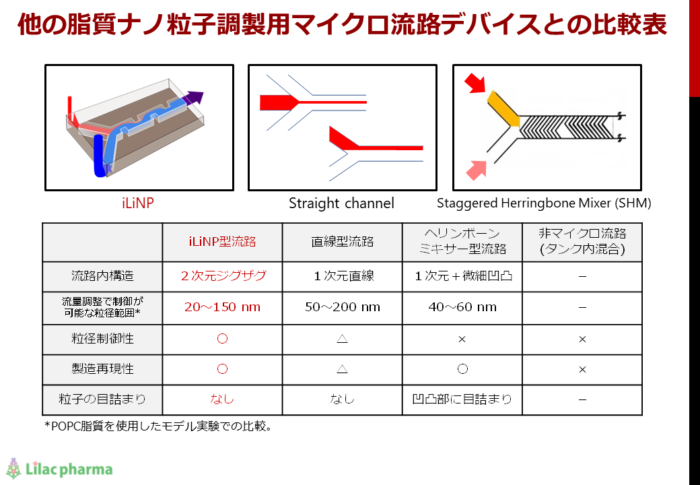
ライバルのマイクロ流路に勝るiLiNPの粒径コントロール性能
リポソーム・ミセル製造用のマイクロ流路としては、弊社のiLiNPの他に、カオティックミキサー(別名:スタッガードヘリンボーンミキサー:SHM)と呼ばれる複雑な3次元凹凸を持つものや、真っ直ぐな流路形状のものがあります。
カオティックミキサーは撹拌混合能力に優れているため、比較的低流速でも極小サイズのリポソーム・ミセルを作ることが可能ですが、流量(流速)変化による粒径コントロールが苦手です。
真っ直ぐな流路形状のものは性能がiLiNPに似ていますが、液体の混合を促進する部分が無いため小さな粒子を作るのが苦手です。
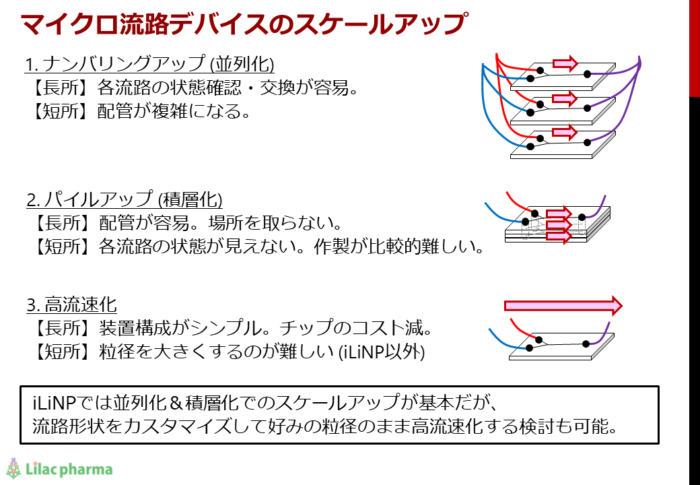
スケールアップは容易
流路幅がμmオーダーのデバイスを使用する関係で、デバイス1枚あたりの生産量はどうしても少量になってしまいます。しかしデバイスを並列化することでこの問題を克服できます。
更に、バッチ法では反応容器の大きさが変わると熱伝導や撹拌効率が変わるため、その都度、製造条件の再検討が必要ですが、iLiNPでのスケールアップは製造条件が決まったデバイスを複数枚並べるだけなので、同じ流量で流すことさえできれば、製造条件の再検討は要りません。またバッチ法と異なり連続生産プロセスなので、24時間無人で流し続けリポソームを作り続けることも原理的には可能です。
これらの工夫により、バッチ法に劣らない生産効率を達成することも不可能ではありません。
広がるiLiNPの可能性
iLiNPによってリポソーム・ミセルの粒径を自由にコントロールできるようになり、これまで実は十分な効果が得られていなかったリポソーム医薬品やリポソーム配合化粧品なども、今後はその効果を最大限に発揮できる可能性が大きくなりました。このことは即ち、従来治らなかった難病を克服し、また迫りくる老いを感じさせなくすることがiLiNPによって可能となり、ひいては全世界の皆様に、希望に満ちた未来を与えることが可能となります。
また医薬品、化粧品に限らず、様々な分野でのiLiNPの活用が今後期待されます。リポソーム・ミセルは既に、研究用試薬の他、検査薬、サプリメントなどにも使われています。
リポソーム・ミセルは古くより知られているカプセル素材で、そのポテンシャルを追求する様々な研究開発が長年行われています。その結果、リポソームの素材となる脂質についてはバラエティに富んだものが生まれ、特に医薬品の分野でその利用が始まっていますが、製造技術、特に粒径制御についてはこれまで大きなブレークスルーがありませんでした。そのような中、マイクロ流路技術、特にiLiNPのような優れた製造技術が生まれたことにより、これまで想像できなかった未知のリポソーム・ミセルの利活用が期待されます。もし新しいアイデアがあれば、ぜひとも弊社にご連絡ください。一緒に希望に満ちた未来を作りましょう。

